Ein Lösungsanbieter für verschiedene Herausforderungen der Primärverpackungen im mRNA-Lebenszyklus
Auswahl von Fläschchen für die schnelle Markteinführung oder PFS für einfache Bedienung und Flexibilität. Die branchenüblichen vorfüllbaren syriQ® Glas Spritzen haben sich bei Temperaturen von bis zu -50 °C bewährt und die vorfüllbaren SCHOTT TOPPAC® Polymer Spritzen bei bis zu -180 °C. Wir haben die Lösung um Ihre Anforderungen zu Lagerung und Transport zu unterstützen.
mRNA Anwendungen sind eine Herausforderung für die Primärverpackung
Die anspruchsvollen Lagerungs- und Transportbedingungen von mRNA Anwendungen unter niedrigen Temperaturen stellen eine zusätzliche Belastung für die Primärverpackung dar. Die Bedingungen in niedrigen Termperaturen und der Frost-Tau-Zyklus können sich auf die mechanische Stabilität, die Performance die Container Closure Integrity des Behälters sowie die Partikellast auswirken. All diese potenziellen Risiken müssen verstanden und beachtet werden, um ein mRNA Medikament mit dem notwendigen Vertrauen auf den Markt zu bringen.
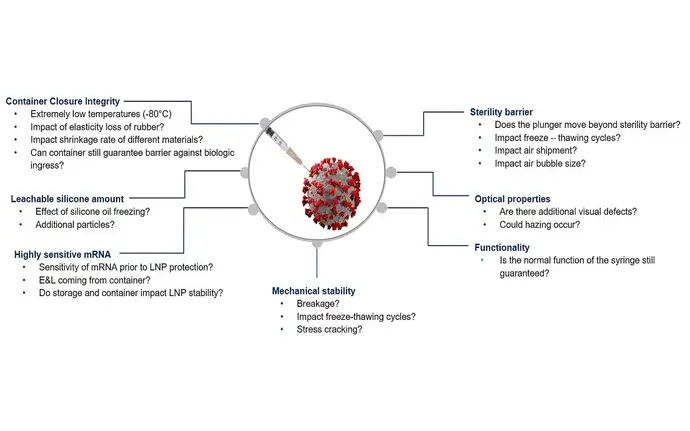
Welche Herausforderung Ihre mRNA Anwendungen auch bereit hält, SCHOTT Pharma unterstützt Sie dabei.
Schnelle Markteinführung? Nutzung einer PFS für mehr Benutzerfreundlichkeit? Extrem kalte und schwierige Liefer- und Lagerbedingungen? Probleme mit Arzneimittelbehälter-Wechselwirkungen? Technische und unvoreingenommene Unterstützung?
Daten und Ergebnisse
Testdaten zu verschiedenen Themen wie Sterilität, CCI, potenzielle Arzneimittelbehälter-Wechselwirkungen oder Funktionalität helfen, die Aspekte des sicheren Verpackens von mRNA besser zu verstehen.
Polymerspritzen eignen sich ideal für mRNA-Anwendungen bei niedrigen Temperaturen.
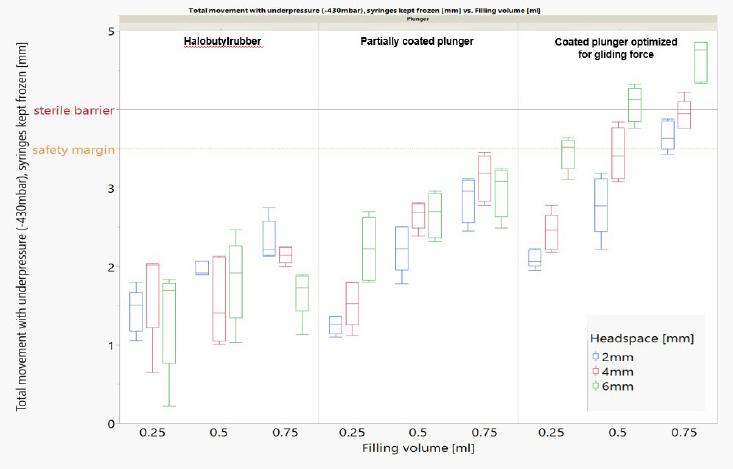
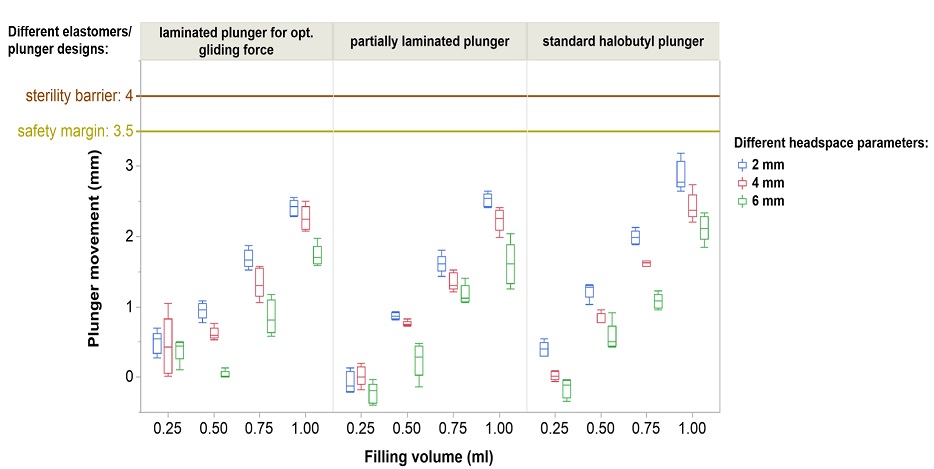
Die Sterilbarriere kann mit den richtigen Spritzenkomponenten und F&F-Parametern kontrolliert werden.
*Die Größe des Verschlussabstands, der Kolbentyp sowie das Füllvolumen wirken sich auf die Kolbenbewegung aus.
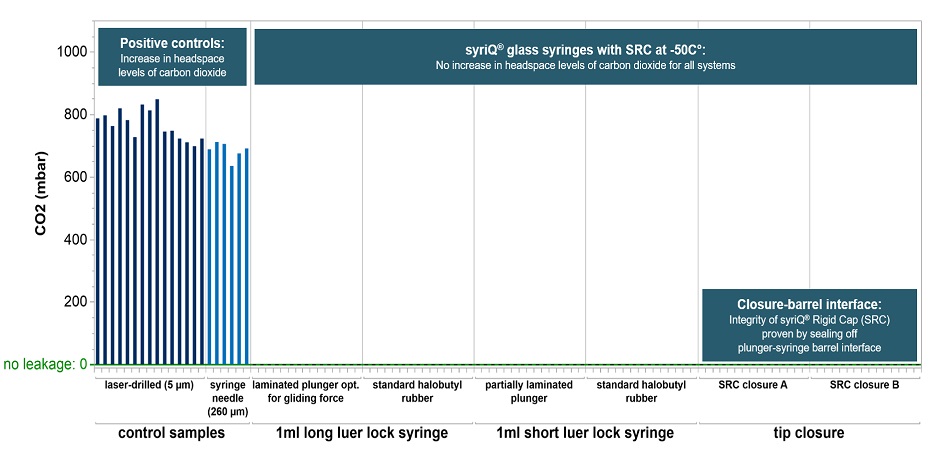
Die Container Closure Integrity (CCI) des Behälters bleibt auch bei -180 °C erhalten.
Geringeres Risiko für Arzneimittelwechselwirkungen und für unsichtbare Partikel durch vernetzte Silikonisierung.
| Uhrzeit | Freies Silikon [mg/l] 3x gefroren bei -20 °C und aufgetaut |
Freies Silikon im Vergleich zum Standard SCHOTT TOPPAC® |
Freies Silikon [mg/l] , gelagert bei 5°C |
Freies Silikon im Vergleich zum Standard SCHOTT TOPPAC® |
|||
|---|---|---|---|---|---|---|---|
| SCHOTT TOPPAC® vernetzte Silikonierung Standardmäßiges vernetztes Silikon |
0d | 0,23 | entf. | < 0,2 | entf. | ||
|
SCHOTT TOPPAC® aufgesprühte Silikonierung Aufgesprüht auf DC360, 0,55 mg/Barrel |
0d | 5,6 | 24 Mal | 1,09 | 5 Mal | ||
*Nach drei Tau- und Gefrierzyklen bei -20 °C steigt die Menge des herausgetretenen Silikons bei beiden Silikonisierungstechnologien, aufgesprühtes Silikon ist jedoch erheblich stärker betroffen. Wir sehen 24-mal mehr freies Silikonöl für die silikonisierte Spritze bei aufgesprühter Silikonisierung. Die Schmiertechnik hat Einfluss auf die Arzneimittelstabilität. Eine immobilisierte, vernetzte Silikonisierung senkt das Risiko von Arzneimittelwechselwirkungen.
Normale Funktionalität der Spritze auch bei -180 °C.
Alle normalen Funktionen der Polymerspritze bleiben nach 3-maligem Einfrieren/Auftauen unverändert und es wurden nach mehreren Studien keine Restrisiken festgestellt:
- Keine Änderung der Transparenz
- Keine Beeinträchtigung der mechanischen Stabilität
- Keine Veränderung des optischen Erscheinungsbildes
*Bei den verschiedenen Temperaturen wurde kein Unterschied bei der Injektionsleistung (Break-Loose&Gliding force) beobachtet und die Ergebnisse waren vergleichbar mit denen von Spritzen, die bei Raumtemperatur gelagert wurden. Das Ansetzen eines Tau-Gefrierzyklus hat keinen wesentlichen Einfluss auf die Funktionalität.
Vorfüllbare Glasspritzen, die sich ideal für mRNA-Anwendungen bei niedrigen Temperaturen von bis zu -50 °C eignen.
Keiner der hier gezeigten getesteten Kolben durchbricht die Sicherheitsgrenze: Tiefkalte Temperaturen haben einen komplexen Effekt auf die Kolbenbewegung. Wir haben die Integrität der Sterilbarriere mit verschiedenen kontrollierten Fill-and-Finish Parametern nachgewiesen.*
*syriQ® 1 ml lange Glasspritze mit SRC; WFI als hier abgebildetes Füllmedium. Daten für andere Systeme verfügbar.
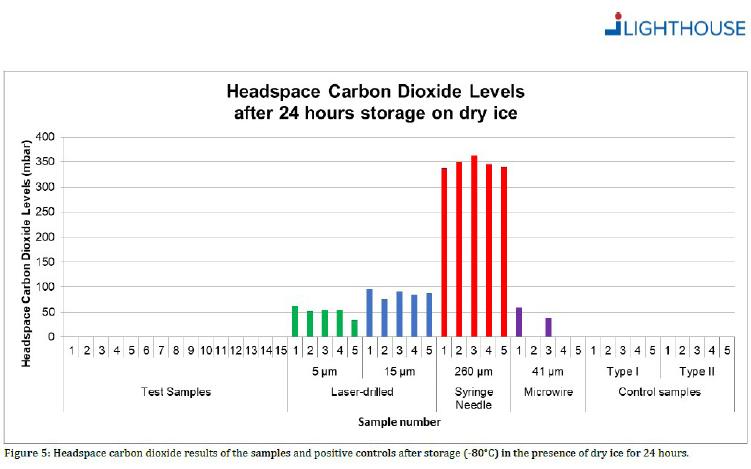
Eine weitverbreitete Testmethode*, die auf der Headspace-Analyse basiert, hat die Container Closure Integrity bei Temperaturen von bis zu -50 °C für verschiedene vorfüllbare Spritzensysteme (PFS) aus Glas nachgewiesen.
* Für jedes PFS-System wurden 15 leere Spritzen für 24 Stunden auf Trockeneis bei -50 °C gelagert. Die Spritzen wurden mit dem qualifizierten °Lighthouse Instruments FMS-Carbon Dioxide Headspace Analyzer (Modell FMS-CO2) getestet. Keine der Testproben zeigte Anzeichen von CO2-Eintritt.
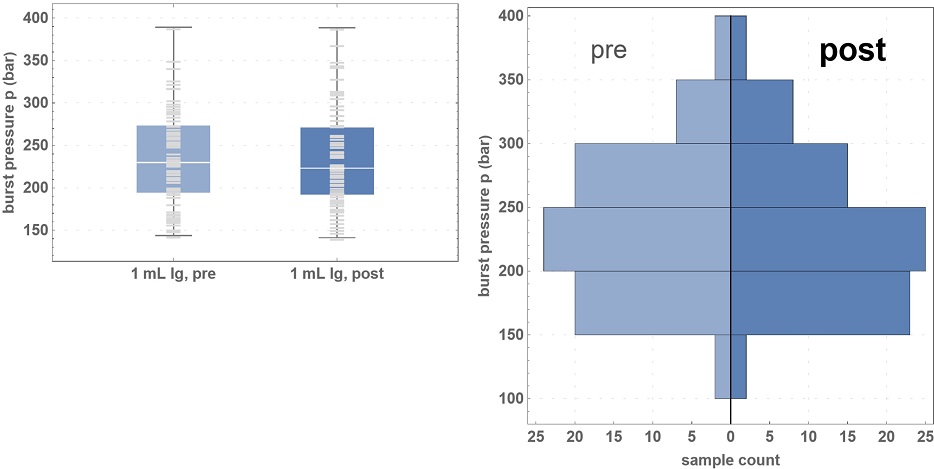
Die Berstdruckergebnisse zeigen, dass die mechanische Festigkeit über den Frost-Tau-Zyklus hinweg stabil ist.*
*75 Spritzen wurden vor und nach dem Einfrieren bei -50 °C getestet, wobei Puffer und ein Frost-Tau-Zyklus verwendet wurden, um die Kühlkette für mRNA zu simulieren.
Die Drehmomentstärke und die Konnektivität des Luer Lock Adapters wurden nicht beeinträchtigt, und bei 900 Spritzen konnten wir keine Veränderungen der optischen Eigenschaften feststellen.
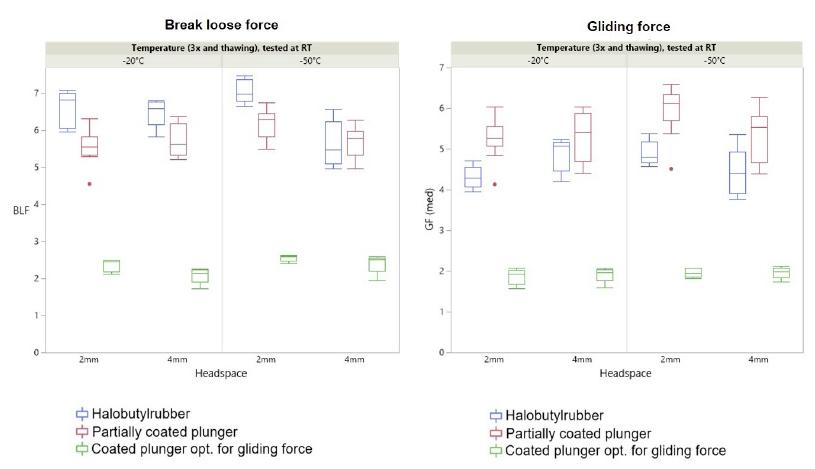
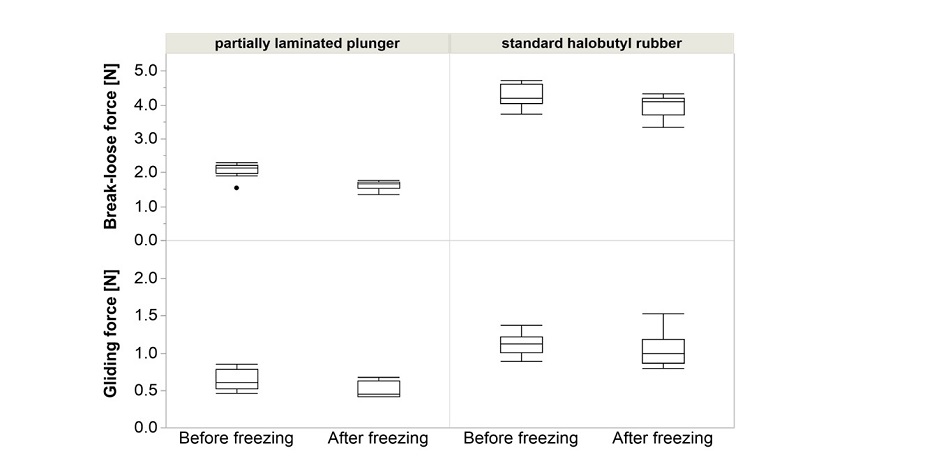
Die Injektionsleistung (Break-Loose & Gliding force, BLGF) von syriQ® Glasspritzen wird nach dem Frost-Tau-Zyklus im tiefkalten Temperaturbereich nur minimal beeinträchtigt.
*Beispiel: syriQ® 1 ml lange Glasspritze mit SRC; Daten für andere Systeme verfügbar.
SCHOTT Pharma als richtiger Partner für die mRNA-Technologie
- Optimale Lösungen für die Aufbewahrung von Medikamenten in jeder Phase des Lebenszyklus: von Fläschchen bis hin zu vorfüllbaren Spritzen.
- Unvoreingenommene Beratung und Unterstützung für vorfüllbare Spritzen je nach Bedarf der Anwendung.
- SCHOTT Pharma Services testet die Kompatibilität von Arzneimittelbehältern für mehrere Medikamente.